【研究背景】
迄今为止,虽然商用锂离子电池已经非常成功,但它们在能量密度、价格和环境友好性方面难以令人满意。锂硫(Li-S)电池是十分有希望的替代品,因为正极采用无毒、含量丰富的硫粉。同时,Li-S电池具有极高的理论能量密度,远远超过商用正极材料。
针对Li-S电池中存在的穿梭效应问题,近年来提出的高浓度电解质可抑制多硫化物的溶解。然而,高浓度电解质同样带来高粘度和离子迁移率低等问题,在高载硫量和高倍率下,限制了活性物质的利用。其次,高电解质粘度还需要更长的电极润湿时间,这不利于电池生产制造。最后,高浓度电解质还使用大量相对昂贵的锂盐,这降低了电池的比能量,增加了电池成本。相比之下,低浓度电解质很少受到关注,因为它们可能会提高多硫化物的溶解性,导致更严重的穿梭效应。
【文章简介】
佐治亚理工学院Feixiang Wu、Gleb Yushin合作,以“Tuning Low Concentration Electrolytes for High Rate Performance in Lithium-Sulfur Batteries”为题,在Journal of The Electrochemical Society发表最新成果,探索不同盐和盐混合物的低摩尔电解质,并研究其物理性质如何影响锂硫电池的性能(容量、内阻,以及循环稳定性)。
【文章解读】
1. 物理性质
对于电解质,随着盐浓度的增加,其粘度增加。所有低浓度电解质的总盐浓度为0.2M,且显示出类似的粘度?0.5mpa·s(图1a)。当LITFSI盐浓度增加到1M时,粘度增加了三倍,达到1.5mpa·s,其中以3M LITFSI的粘度最大,达到42.5mpa·s。图1b显示,虽然使用较高浓度的1M电解质比使用较低浓度电解质产生的欧姆电池电阻稍低,但与锂片的整体界面电阻明显较高。虽然低电解液电阻很重要,但锂负极界面的低电阻和快速动力学影响更为明显。3M LiTFSI的欧姆电阻更高(图1c),但界面电阻更低,而0.1M LiPF6电解质的界面电阻最低(图1d)。
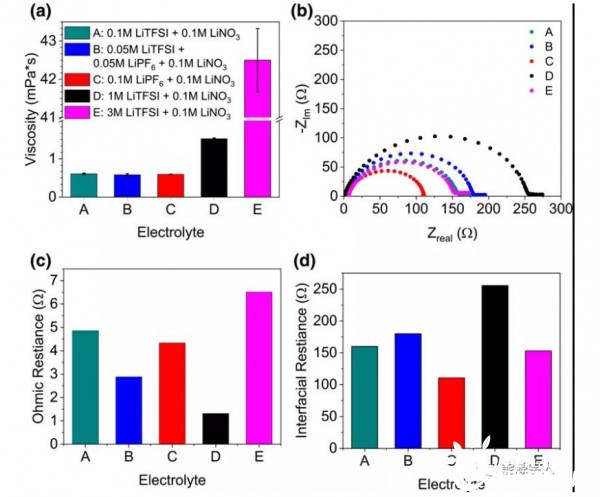
图1 电解质的物理性质(a)粘度,(b)Li/Li对称电池的EIS,(c)欧姆电阻,(d)Li界面电阻。
接触角测量(图2)显示了0.1MLiTFSI、1M LiTFSI和3M LiTFSI样品(A、D和E)的结果。剩下的电解质(样品B和C)太易挥发,不能形成一滴。1MLiTFSI接触角仅略高于0.1M LiTFSI,3MLiTFSI则是两者接触角的两倍以上。样品A、D和E分别用1.5、3和10秒浸润在电极中,与粘度数据相匹配。

图2 接触角测量。
2. 电化学测试
图3显示了低浓度电解质的电化学性能。在低浓度电解液和1M LiTFSI中,低浓度电解液在倍率上的性能相似,0.1M LiTFSI电解质表现最差。图3b显示了每个电解液的C/10充放电曲线,所有低浓度电解液都表现出平坦的平台、低滞后和低极化。同样,在2C(图3c)下,反应仍然正常进行,虽具有更高的滞后,但没有明显的动力学限制。长循环测试(图3d)表明,混合LiTFSI/LiPF6电解质的容量衰减最低。0.1M的LiTFSI电解质具有较高的初始容量,但不太稳定,如0.1M的LiPF6一样。
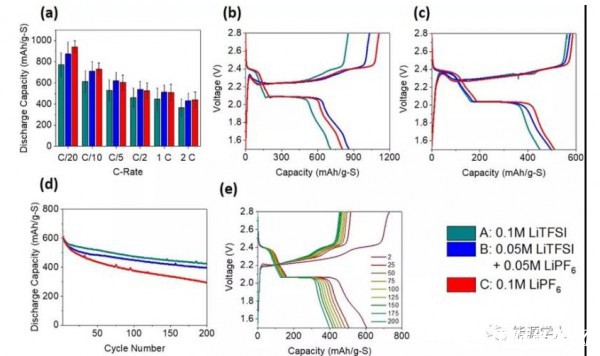
图3 低浓度电解液的电化学结果(a)倍率测试,(b)C/10充放电,(c)2 C充放电,(d)C/5循环稳定性,(e)0.05MLiTFSI+0.05M LiPF6电解液的充放电曲线变化。
低浓度电解质样品A、B和C显示出与1M LiTFSI电解质相似的容量和电压滞后,表明盐浓度高于0.1–0.2M(至约1M)可能是不必要的电解质重量和成本增加。样本B在C倍率上的表现与D相似或更好(图4a-c)。在误差范围内,1M和低浓度电解质之间的差异不显著,因此,更轻、更便宜的低浓度电解质可在不牺牲性能的情况下取代1M LiTFSI电解质。即使相对较薄的电极,高浓度电解质(3M LiTFSI样品E)也能实现最高容量,但它也具有更高的极化、更高的电阻和低效转化反应。而且,如前所述,它的粘度过高、成本增加。相比之下,较便宜且粘度较低的电解质A-C提供更平坦的平台、显著较低的迟滞以及与传统的1M LiTFSI(样品D)类似或更好的容量。
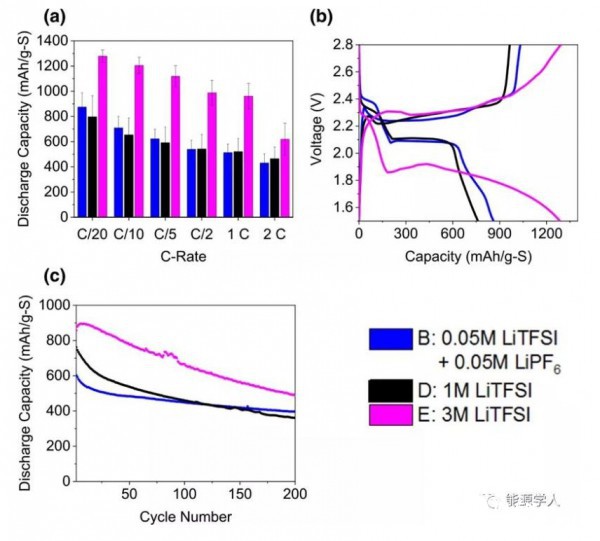
图4 最佳低浓度电解质和高浓度电解质的电化学结果比较(a)倍率测试,(b)C/10充放电,(c)C/5循环稳定性。
对比长循环前后的EIS结果(图5),发现0.1M电解质的阻抗降低幅度最大。然而,3M电解质在循环后表现出最大的阻抗和最大的界面电阻。
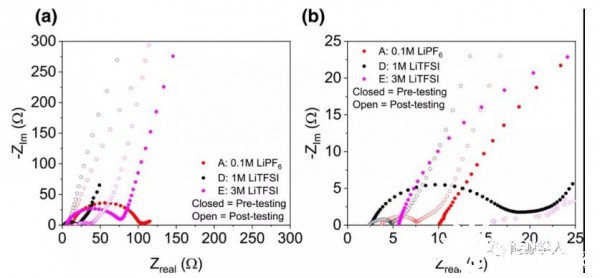
图5(a)0.05MLiTFSI+0.05M LiPF6电解液与1M和3M LiTFSI电解液(均为0.1M LiNO3/DME+DIOX)的EIS结果比较;(b)高频区放大图。
3. SEM/EDS结果
对测试的S-KB正极进行的测试后SEM分析表明,所有样品的微观结构变化非常小(图6)。单个碳颗粒在形貌上无变化且无厚的表面层(例如CEI或再沉积(聚)硫化物或S),可能与多孔KB颗粒非常高的外表面积和相对较小的电极负载有关(图6)。锂负极(图7a-c)一侧,在循环后出现了显著的变化。图7d、7e显示了2C放电结束时,锂片的EDS结果。与低浓度和高浓度电解质相比,1M电解质产生最大强度的N、F和S,表明最大的硫溶解和最厚的SEI形成。LiTFSI、LiPF6混合电解质的F强度比0.1M LiTFSI电解质的F强度大,这是由LiPF6分解产生的额外F引起的。

图6(a)原始电极和在(b)0.1M LiTFSI,(C)0.05MLiTFSI+0.05M LiPF6,(d)1M LiTFSI中循环后的SEM图。
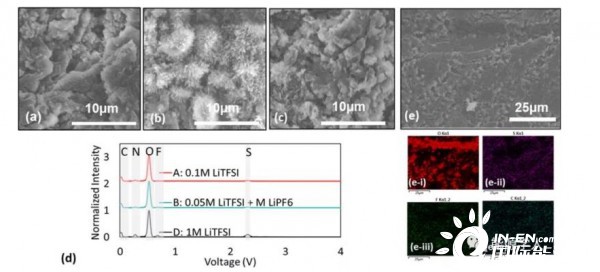
图7(a)0.1M LiTFSI,(b)0.05M LiTFSI+0.05M LiPF6,(C)1M LiTFSI电池,(d)Li箔的EDS图,(e)在0.05M LiTFSI+0.05M LiPF6中测试后的Li箔的EDS图。
4. XPS结果
对测试后正极(图8)的XPS分析表明,在所有电解质成分的情况下,LiTFSI盐和电解质溶剂的分解与CEI的形成略有不同。对于低浓度电解质,CEI种类主要包括:CFn、LiF、含N化合物、亚硫酸盐,和硫酸盐(图9)。总的来说,电解液中即使有1/10–1/3的盐浓度,显然也足以再现在1M和3M电解液组成中形成的保护性CEI的组成。含有0.05–0.1M LiF6的电解质显示出较低的CF2强度,而大多数LiTFSI电解质具有较高的LiF与CFn。有趣的是,只有由0.05M LiPF6和0.05M LiTFSi组成的电解液中含有最明显的Li3N,这是一种对电极保护非常重要的化合物。
与1M和3M号电解质相比,低浓度电解质的含氮化合物比含氮有机化合物多。这可能是由于在低浓度电解质中LiNO3的相对比例较高。只有0.1M LiTFSI同时具有CF2和CF3键,而所有电解质都显示出C–C、C–H、C–O和C=O键,这与二氧环烷溶剂的分解和聚合一致。
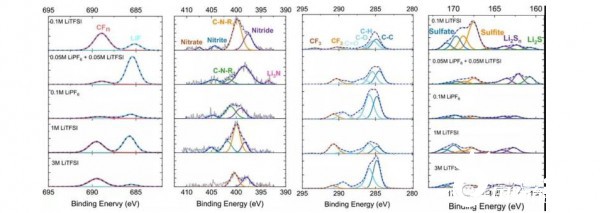
图8 全部电解质硫正极的XPS结果。
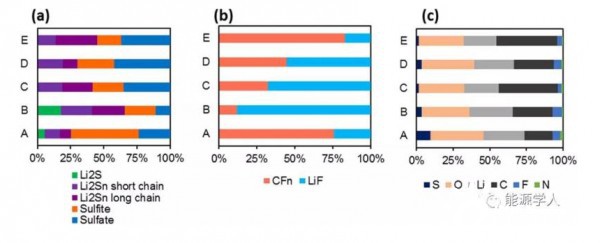
图9 定量分析循环后硫正极的XPS峰。
【结论】
该研究工作将两种常见的电解质盐LiTFSI和LiPF6,在低浓度下进行组合,结果表明它们的组合产生的容量与传统的1M LiTFSI电解质相当。与最初的预期相反,将电解液浓度从1M降低到0.2M并没有增加锂负极上的多硫化物溶解和Li2S沉积。事实上,倍率和长循环测试都显示低浓度电解质的性能与标准1M电解质相似或更好。其次,低浓度电解质能够实现更低的成本和更高的能量密度,因此,对其可进一步深入研究。
 切换行业
切换行业







 正在加载...
正在加载...




